Гемоглобин содержит: Что такое гемоглобин, его виды и формы :: Здоровье :: РБК Стиль
РазноеЧто нужно знать о HbA1C
Среди множества цифр результатов анализов, которые подготавливают врачи, простое значение анализа HbA1C может помочь выяснить, насколько хорошо вам удается следить за уровнем сахара крови.
Прежде всего давайте выясним, что такое HbA1C?
Вы можете встретить различные названия данного показателя:
- A1c
- Гликированный гемоглобин
- Гликозилированный гемоглобин
- Гемоглобин A1C
Уровень HbА1С (гликированного гемоглобина) показывает, какой процент гемоглобина в эритроцитах связывается с глюкозой1. Так как время жизни эритроцита, который содержит гемоглобин, составляет несколько месяцев, анализ HbА1С позволяет установить, насколько эффективен был контроль уровня сахара крови в предшествующие 2-3 месяца.
С какой периодичностью необходимо проверять уровень HbА1С?
Американская диабетическая ассоциация (ADA) рекомендует пациентам с сахарным диабетом со стабильным уровнем сахара крови делать анализ HbА1С каждые полгода, а если не удается добиться намеченного уровня сахара крови или необходимо изменить проводимое лечение, такой анализ выполняется каждые 3 месяца
К какому уровню HbА1С необходимо стремиться?
В соответствии с рекомендациями Американской диабетической ассоциации, необходимо добиваться того, чтобы уровень HbА1С составлял 7% или ниже, и чем ближе этот показатель будет к 6% без риска для здоровья, тем лучше. Однако для каждого человека этот уровень должен устанавливаться в зависимости от состояния здоровья на текущий момент и с учетом многих факторов (в частности, чувствует ли человек наступление гипогликемии). Скорее всего, если ваш уровень HbА1С превышает 7%, то врач посоветует вам, что нужно сделать, чтобы снизить его, ведь кроме всего прочего снижение этого показателя способствует уменьшению риска отдаленных осложнений диабета, которые мы стремимся предотвратить 2.
Можно ли обойтись без измерения уровня сахара в крови, если сделан анализ HbА1С?
Так как уровень HbА1С является усредненной величиной, он не может гарантировать, что показатели сахара в крови в течение дня находятся в безопасном диапазоне. Давайте посмотрим, что значит усредненная величина. Средним числом для чисел 5-5-5-5 и чисел 1-9-1-9 будет число 5, однако на графике числа 1-9-1-9 будут выглядеть как резкие подъемы и спады. Это касается и уровня сахара в крови. При наличии множества резких подъемов и спадов после усреднения уровень HbА1С может быть похожим на уровень HbА1С здорового человека3.
Давайте посмотрим, что значит усредненная величина. Средним числом для чисел 5-5-5-5 и чисел 1-9-1-9 будет число 5, однако на графике числа 1-9-1-9 будут выглядеть как резкие подъемы и спады. Это касается и уровня сахара в крови. При наличии множества резких подъемов и спадов после усреднения уровень HbА1С может быть похожим на уровень HbА1С здорового человека3.
Поэтому правильнее всего оценивать результаты анализа на HbА1С при наличии результатов самостоятельного контроля уровня сахара в крови. Нельзя понять, как развивается заболевание, если не проводить самоконтроль уровня сахара в крови.
Если уровень HbА1С низкий, имеют ли значение колебания уровня сахара в крови?
Уровень сахара в крови, как правило, меняется в течение дня, и это связано с тем, что мы едим, сколько двигаемся и отдыхаем. В настоящее время наряду с результатами анализа HbА1С оценивается и высокая вариабельность гликемии — так называются эти колебания уровня сахара в крови.
Данные, полученые в исследовании, посвященном лечению и осложнениям диабета (Diabetes Control and Complications Trial, DCCT4), показали, что при одинаковом уровне HbА1С более подвержены определенного рода осложнениям те пациенты, у которых отмечаются более выраженные колебания уровня сахара в крови.
Если вы хотите узнать, попадаете ли вы в группу риска и как ваши действия влияют на уровень сахара в крови, то с помощью Формы Акку-Чек 360° (Анализ уровня глюкозы в крови: до и после еды) вы сможете понять, как еда, физическая нагрузка, лекарства, стресс или болезнь могут влиять на уровень сахара в течение дня. Доказано, что эта система анализа даже помогает снизить уровень HbA1C, если работать по ней вместе с врачом 5. Начните перемены к лучшему прямо сейчас.
Гематоген Народный с черносливом 40г
Гематоген «С черносливом» дополнительно содержит кусочки чернослива, которое обладает отличными вкусовыми качествами, содержит волокна.
Гематоген – биологически активная добавка (БАД) к пище, не является лекарством. Название продукта «Гематоген» в переводе с греческого — «рождающий кровь». Основной компонент гематогена — это гемоглобин, который стимулирует кроветворение.
Гемоглобин (альбумин пищевой черный) представляет собой красный порошок – продукт сушки крови крупного рогатого скота. Это высокобелковый препарат, содержащий около 90% белковых веществ. Основная составляющая – белок гемоглобин, который и определяет функциональные свойства гематогена. Гемоглобин – белок эритроцитов, красных кровяных клеток, переносящий молекулярный кислород от легких к тканям в организмах позвоночных животных. Состоит из ГЕМА (красящего вещества), представляющего собой комплексное соединение Fe (II) и белка – глобина. Ценность (эффективность) содержащегося в Гематогене гемоглобина заключается в том, что железо в нем находится в наиболее усвояемой для человека форме (в отличие от железа, содержащегося в растительной пище). Благодаря этому оно лучше всасывается в желудочно-кишечном тракте и быстрее включается в обменные процессы организма человека. Гемоглобин (альбумин пищевой черный) является обязательной составляющей всех видов Гематогена.
Это высокобелковый препарат, содержащий около 90% белковых веществ. Основная составляющая – белок гемоглобин, который и определяет функциональные свойства гематогена. Гемоглобин – белок эритроцитов, красных кровяных клеток, переносящий молекулярный кислород от легких к тканям в организмах позвоночных животных. Состоит из ГЕМА (красящего вещества), представляющего собой комплексное соединение Fe (II) и белка – глобина. Ценность (эффективность) содержащегося в Гематогене гемоглобина заключается в том, что железо в нем находится в наиболее усвояемой для человека форме (в отличие от железа, содержащегося в растительной пище). Благодаря этому оно лучше всасывается в желудочно-кишечном тракте и быстрее включается в обменные процессы организма человека. Гемоглобин (альбумин пищевой черный) является обязательной составляющей всех видов Гематогена.
Гематоген традиционно используется при лечении пониженного уровня железа в крови у детей (в медицине это состояние называется «железодефицитная анемия»). Следствием железодефицитных состояний является ухудшение функционального состояния различных систем и органов человека, в том числе снижение иммунной резистентности (устойчивости), замедление умственного и физического развития детей.
Следствием железодефицитных состояний является ухудшение функционального состояния различных систем и органов человека, в том числе снижение иммунной резистентности (устойчивости), замедление умственного и физического развития детей.
Показания: Рекомендуется в качестве дополнительного источника железа.
И так основная польза Гематогена:
- Стимуляция кроветворения
- Чудесная добавка к пищевому рациону
- Источник витаминов, микро- и макроэлементов.
Состав: сахар-песок, молоко сгущенное с сахаром (молоко нормализованное, сахар, лактоза), патока крахмальная, кусочки чернослива, альбумин пищевой черный (гемоглобин), железо (II) сульфат, ароматизатор натуральный «ваниль».
Противопоказания: индивидуальная непереносимость компонентов, нарушение углеводного обмена.
Способ применения: детям 3-6 лет – 30 г в день; с 7 лет – 40 г в день; взрослым — 50 г в день. Принимать во время еды. Продолжительность приема 3-4 недели. Перед применением рекомендуется проконсультироваться с врачом.
Принимать во время еды. Продолжительность приема 3-4 недели. Перед применением рекомендуется проконсультироваться с врачом.
Форма выпуска: Гематоген выпускается штучно, в виде плиток коричневого или темно-коричневого цвета, сладкого вкуса весом 40 г, деленных на дольки.
Условия и сроки хранения: в сухом, защищённом от попадания прямых солнечных лучей, недоступном для детей месте, при температуре не выше +25°С.
Условия отпуска из аптек: без рецепта.
Срок годности: 8 месяцев.
Зачем нужен гемоглобин и какие продукты помогут его повысить
Уровень гемоглобина в крови очень важен для работы всего организма, поэтому его следует поддерживать.
Из школьного курса биологии многие в общих чертах помнят, что такое гемоглобин. Понятно, что он содержится в крови, и очень важно для здоровья поддерживать его уровень. Но каковы его главные функции, к чему может привести его низкий уровень и как это уровень поднять, благодаря продуктам из холодильника?
Важность железа
Для производства крови организму необходимо одно очень важное вещество – железо. Примерно 70 процентов этого вещества содержится в красных кровяных тельцах или гемоглобине, часть – в мышечных клетках, которые называются миоглобином. Гемоглобин участвует в процессе переноса кислорода в крови, который поступает от легких к тканям. А миоглобин принимает, хранит, транспортирует и выделяет кислород в мышечных клетках.
Примерно 70 процентов этого вещества содержится в красных кровяных тельцах или гемоглобине, часть – в мышечных клетках, которые называются миоглобином. Гемоглобин участвует в процессе переноса кислорода в крови, который поступает от легких к тканям. А миоглобин принимает, хранит, транспортирует и выделяет кислород в мышечных клетках.
Анемия
В организме среднего взрослого мужчины около 1000 мг запасенного железа, которого хватает на три года. Средняя взрослая женщина имеет только 300 мг, которых вполне достаточно на полгода. Гемоглобин в организме снижается, когда человек перестает потреблять это самое железо и его запасы заметно истощаются. Это может привести к кислородному голоданию тканей или железодефицитной анемии, что также является дополнительной нагрузкой на сердце. Еще одной причиной истощения может быть кровопотеря. Особенно это касается женщин, которым необходимо поддерживать уровень гемоглобина в крови во время менструаций.
Суточная норма
Важно понимать, что железо не вырабатывается в организме самостоятельно.
В каких продуктах содержится железо
В этот список входит говядина, телятина, свинина, ягненок, курица, индейка – в идеале готовить на пару. Отлично подойдет печень: говяжья, куриная, свиная, но не выбирайте печень рыбы.
Наиболее богаты железом – гранат, тофу, брокколи, горошек, брюссельская капуста, яблоки, ростки фасоли, помидоры, бобы фасоли, картошка, стручковая фасоль, кукуруза, свекла, капуста
Отлично подойдут тунец и лосось, моллюски и устрицы, а также красная, черная и желтая икра.
Трехмерная научная модель гемоглобина
Организация транспорта кислорода в многоклеточном организме является крайне важной эволюционной задачей, поскольку этот газ нужен каждой клетке для окисления биомолекул и получения энергии, а его растворимость в воде недостаточна для эффективного переноса нужных количеств. Транспортер на основе атомов железа, координированных сложной органической группой и окруженных белковой глобулой оказался наиболее эффективным эволюционным приспособлением для решения этой задачи. Гемоглобин стал одним из самым изучаемых белков XX века — первым, для которого была полностью описана пространственная структура и детальный механизм работы.
Строение и работа гемоглобина
Гемоглобин — это сложный белок эритроцитов человека и животных, необходимый для осуществления транспорта кислорода и оксида углерода IV кровью. Существует несколько форм этого белка. Гемоглобин А, встречающийся в организме взрослых людей, состоит из двух α и двух β субъединиц, каждая из которых содержит гем, в состав которого входит атом железа, что и придает эритроцитам и крови человека красный цвет [1].
Существует несколько форм этого белка. Гемоглобин А, встречающийся в организме взрослых людей, состоит из двух α и двух β субъединиц, каждая из которых содержит гем, в состав которого входит атом железа, что и придает эритроцитам и крови человека красный цвет [1].
Белок устроен таким образом, что в условиях высокой концентрации кислорода (в капиллярах легких) он легко присоединяет молекулы O2. При этом каждая присоединенная молекула делает связывание остальных O2 проще. Обратная ситуация имеет место в тканях, где, благодаря повышенному содержанию растворенного углекислого газа, создается более кислая среда. В таких условиях гемоглобин, легко отдавая связанный кислород. Гемоглобин является аллостерическим белком. Связывание первой молекулы кислорода с одной из субъединиц этого белка провоцирует конформационные изменения в других субъединицах, что влияет на связывание остальных молекул кислорода и увеличивает эффективность превращения дезоксигемоглобина в оксигемоглобин.
 На каждый эритроцит приходится порядка 280 миллионов молекул этого белка (96% сухого веса). При объеме крови в 5 литров, общая масса гемоглобина в организме составляет приблизительно 800 грамм. Гемоглобин позволяет растворить в крови в 70 раз больше кислорода, чем можно было бы в его отсутствии (2).
На каждый эритроцит приходится порядка 280 миллионов молекул этого белка (96% сухого веса). При объеме крови в 5 литров, общая масса гемоглобина в организме составляет приблизительно 800 грамм. Гемоглобин позволяет растворить в крови в 70 раз больше кислорода, чем можно было бы в его отсутствии (2).С гемоглобином, помимо кислорода и углекислого газа могут также связываться оксид серы II (SO), оксид азота (NO) сероводород (h3S) и некоторые другие неорганические соединения [3, 4]. Наибольшую опасность для человека представляет способность гемоглобина связываться с угарным газом (СО, оксид углерода II). Эффективность этого процесса в 250 раз выше связывания с кислородом, поэтому вдыхание угарного газа может привести к удушью.
Гемоглобин является одним из наиболее хорошо изученных белков. Он был открыт немецким физиологом Отто Функе в 1851 году, а структуру этого белка описал австрийский молекулярный биолог Макс Перутц в 1959 году, за что тремя годами позднее получил Нобелевскую премию по химии [5].
Показать ссылки
Гемоглобин — это… Что такое Гемоглобин?
Молекула гемоглобина: 4 субъединицы глобина окрашены в разные цветаНормальным содержанием гемоглобина в крови человека считается: у мужчин 130—170 г/л (нижний предел — 120, верхний предел — 180 г/л), у женщин 120—150 г/л; у детей нормальный уровень гемоглобина зависит от возраста и подвержен значительным колебаниям. Так, у детей через 1—3 дня после рождения нормальный уровень гемоглобина максимальный и составляет 145—225 г/л, а к 3—6 месяцам снижается до минимального уровня 95—135 г/л, затем с 1 года до 18 лет отмечается постепенное увеличение нормального уровня гемоглобина в крови. [2]
[2]
Главная функция гемоглобина состоит в переносе кислорода. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало; здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких. Монооксид углерода (CO) связывается с гемоглобином крови намного сильнее (почти в 500 раз), чем кислород, образуя карбоксигемоглобин (HbCO). Некоторые процессы приводят к окислению иона железа в гемоглобине до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от мета… и гемоглобин, иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода. Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в легких.
Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в легких.
Метгемоглобин — производное гемоглобина, в котором железо окислено (трехвалентно). Метгемоглобин не способен переносить кислород. Образуется в организме при некоторых видах отравлений.[3]
Строение
Гемоглобин является сложным белком класса хромопротеинов, то есть в качестве простетической группы здесь выступает особая пигментная группа, содержащая химический элемент железо — гем. Гемоглобин человека является тетрамером, то есть состоит из четырёх субъединиц. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами A-H (От N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Эта простетическая группа нековалентно связана с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две других координационных позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93 положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64 положении цепи (участок E).
Всего в гемоглобине человека четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в легких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь. На эту же связь присоединяется и моноксид углерода, вступая с кислородом в «конкурентную борьбу» за связь с гемоглобином, образуя карбоксигемоглобин.
При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь. На эту же связь присоединяется и моноксид углерода, вступая с кислородом в «конкурентную борьбу» за связь с гемоглобином, образуя карбоксигемоглобин.
Связь моноксида углерода с гемоглобином более прочная, чем с кислородом. Поэтому часть гемоглобина, образующая комплекс с моноксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2 % карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология
Для связывания кислорода с гемоглобином характерна кооперативность: после присоединения первой молекулы кислорода связывание последующих облегчается.
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит.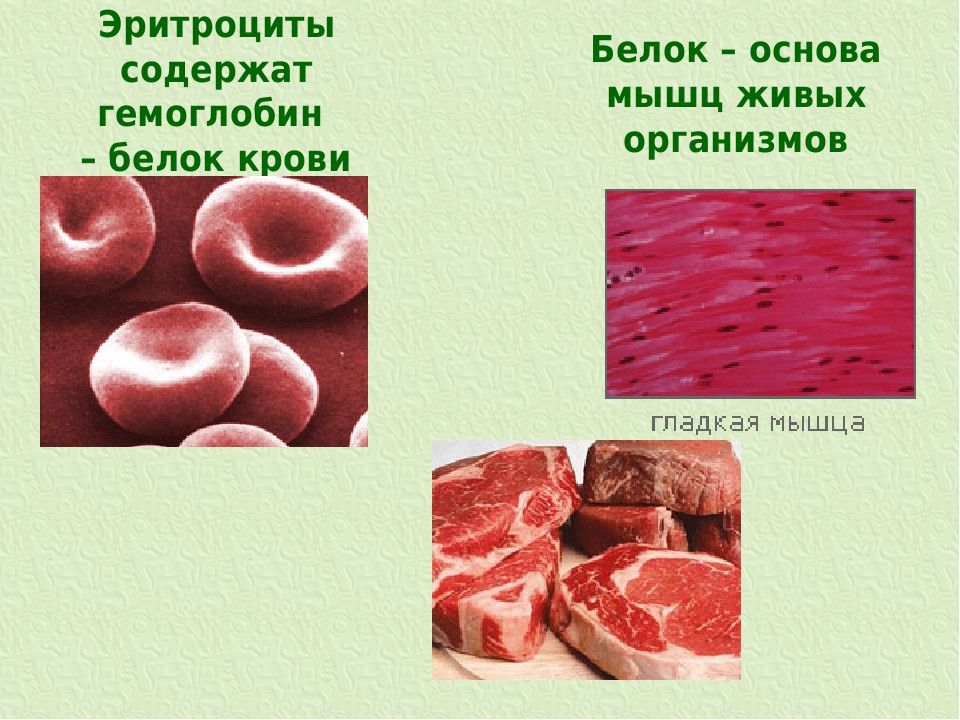 В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидно-клеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидно-клеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высоко токсичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин, специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других желчных пигментов, или выпускается в рециркуляцию в комплексе с трансферрином для повторного использования костным мозгом в процессе эритропоэза.
Экспрессия генов гемоглобина до и после рождения.Также указаны типы клеток и органы в которых происходит экспрессия гена (данные по Wood W.
 G., (1976). Br. Med. Bull. 32, 282.).[4]
G., (1976). Br. Med. Bull. 32, 282.).[4]Гемоглобин при заболеваниях крови
Дефицит гемоглобина может быть вызван, во-первых, уменьшением количества молекул самого гемоглобина (см. анемия), во-вторых, из-за уменьшенной способности каждой молекулы связать кислород при том же самом парциальном давлении кислорода.
Гипоксемия — это уменьшение парциального давления кислорода в крови, её следует отличать от дефицита гемоглобина. Хотя и гипоксемия, и дефицит гемоглобина являются причинами гипоксии.
Прочие причины низкого гемоглобина разнообразны: кровопотеря, пищевой дефицит, болезни костного мозга, химиотерапия, отказ почек, атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается также при поликизэмии (англ.)русск.. Это повышение может быть вызвано: врожденной болезнью сердца, лёгочным фиброзом, слишком большим количеством эритропоэтина.
См. также
Примечания
Литература
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.
 ), Addison Wesley Longman, ISBN 0-8053-3066-6.
), Addison Wesley Longman, ISBN 0-8053-3066-6. - Levitt, M & C Chothia (1976), «Structural patterns in globular proteins», Nature. doi 10.1038/261552a0.
| B05A |
| ||||
|---|---|---|---|---|---|
| B05B |
| ||||
| B05C |
| ||||
| B05D |
| ||||
| B05X |
| ||||
| B05Z |
Железо в крови.
 10 продуктов, которые повысят гемоглобин зимой | ОБЩЕСТВО
10 продуктов, которые повысят гемоглобин зимой | ОБЩЕСТВОСонливость, депрессия, головокружение, слабость в теле… Часто мы наблюдаем у себя эти симптомы зимой. Периодически они возникают из-за нехватки железа в крови. Какие ещё признаки говорят о пониженном гемоглобине и чем нужно питаться в зимнее время, чтобы его поднять — в материале «АиФ на Енисее».
Какая норма?
«Гемоглобин — особый железосодержащий белок в крови, и его нехватка в зимнее время года может понизить иммунитет, вызвать слабость, снизить работоспособность и внимание, увеличить риск возникновения ОРВИ с осложнениями, — рассказывает врач терапевт-гастроэнтеролог Татьяна Майорова. — Но эти симптомы могут перерасти и в более серьёзные заболевания — гепатит, заболевания крови, анемию, туберкулёз, воспаление лёгких и другие».
Определить уровень гемоглобина можно, сдав кровь из вены в поликлинике. Обычно анализ готов через 3-7 дней, результаты озвучивает пациенту лечащий врач. Перед сдачей крови не рекомендуют есть и пить много жидкости. От этого будут зависеть показатели.
Перед сдачей крови не рекомендуют есть и пить много жидкости. От этого будут зависеть показатели.
Некоторые думают, что низкий гемоглобин — временное обстоятельство. Однако следует со всей ответственностью подойти к анализам: вовремя заметить недостаток железа и принять меры по его восполнению. Норма гемоглобина у мужчин: нижняя граница — 120 г/л, верхняя — 160 г/л. У женщин — 114 г/л и 150 г/л соответственно.
Что повысит гемоглобин?
Конечно, в зимнее время года не всегда найдёшь на прилавках магазинов свежие овощи и фрукты, но есть множество продуктов, которые очень быстро помогут поднять уровень железа в крови. О 10 самых полезных и эффективных рассказала консультант по здоровому питанию Наталья Билецкая.
Зимой надо есть как можно больше мяса и печени. Фото: pixabay.com1. Халва. Мало того, что эта восточная сладость полезна для зрения и профилактики онкологических заболеваний, в ней содержится огромное количество железа, влияющего на уровень гемоглобина. Например, тахинная халва содержит 50 миллиграммов на 100 граммов продукта, а подсолнечная — 33 миллиграмма. Лакомство готовят из перемолотых зёрен кунжута, орехов, семян подсолнечника, которые сами по себе отличный источник не только железа, но и витаминов Е, В, фосфора, цинка и кальция.
Например, тахинная халва содержит 50 миллиграммов на 100 граммов продукта, а подсолнечная — 33 миллиграмма. Лакомство готовят из перемолотых зёрен кунжута, орехов, семян подсолнечника, которые сами по себе отличный источник не только железа, но и витаминов Е, В, фосфора, цинка и кальция.
2. Мясо. Каждый человек знает, что зимой надо есть как можно больше мяса. Хороший кусок стейка заправит энергией на полдня, и к тому же вы будете меньше мёрзнуть. Главное, белки животного происхождения помогают прийти в норму клеткам крови. В рационе всегда должны присутствовать говядина, кролик, телятина, печень, язык. Для поддержания нормального уровня гемоглобина достаточно 50 граммов мяса или субпродуктов в день, а для его повышения — не менее 100 граммов в день.
3. Сушёные грибы. Ароматный суп из сушёных грибов — это не только вкусный обед, но и отличное средство для повышения количества железа в организме. В 100 граммах содержится не менее 30 миллиграммов этого вещества. Всего 50 граммов в день — и показатели придут в норму. Качество и безопасность грибов — другой вопрос. Убедитесь, что они не собраны у автомобильных дорог и железнодорожных путей, вблизи сельскохозяйственных угодий и различных свалок.
Всего 50 граммов в день — и показатели придут в норму. Качество и безопасность грибов — другой вопрос. Убедитесь, что они не собраны у автомобильных дорог и железнодорожных путей, вблизи сельскохозяйственных угодий и различных свалок.
4. Морепродукты. Креветки, моллюски, гребешки, кальмары, икра — в морепродуктах целый кладезь витаминов, в том числе и для поддержания гемоглобина. В магазинах вы найдёте в основном замороженные продукты, однако в таком виде большая часть полезных веществ сохраняется.
5. Пшеничные отруби. Они содержат не менее 15 миллиграммов железа на 100 граммов продукта, а также витамины группы В, которые участвуют в синтезе гемоглобина. Отлично подходят для завтрака, но увлекаться ими не стоит. Чтобы не заработать проблем с пищеварительной системой, рекомендуют в день съедать не более 30 граммов отрубей.
6. Морская капуста. Железо, содержащееся в капусте, предотвращает анемию и активирует процесс кроветворения. В профилактических и лечебных целях достаточно съедать в день 2 чайные ложки. Самые популярные и несложные блюда — салаты с добавлением фунчозы, варёных яиц, кукурузы, горошка.
В профилактических и лечебных целях достаточно съедать в день 2 чайные ложки. Самые популярные и несложные блюда — салаты с добавлением фунчозы, варёных яиц, кукурузы, горошка.
7. Свёкла. Очень эффективен натуральный сок или квас из свёклы. Только употреблять его нужно регулярно. Чтобы напиток лучше усваивался, после приготовления рекомендуют подержать его полчаса в холодильнике. К слову, для вкуса можно добавить в него яблочный или морковный сок.
8. Гранат. Уникальный фрукт с множеством полезных витаминов. Пить гранатовый сок нужно регулярно, но в небольших количествах. Желательно не покупать в магазине, а сделать его самостоятельно дома и употреблять в свежем виде. Правда, гранатом не стоит увлекаться при серьёзных проблемах с желудком. В этом случае лучше пить не концентрированный сок, а разбавленный водой.
9. Витаминная смесь из сухофруктов и орехов. Изюм, чернослив, курага, грецкие орехи берутся в одинаковом количестве, тщательно перемешиваются. Получившаяся смесь прокручивается с помощью мясорубки, дополняется небольшим количеством мёда. Есть шесть столовых ложек в день.
Получившаяся смесь прокручивается с помощью мясорубки, дополняется небольшим количеством мёда. Есть шесть столовых ложек в день.
10. Морковный сок. Свежевыжатый морковный сок эффективен в деле подъёма уровня гемоглобина. Пользу организму принесут 300-400 мл в день. Его можно смешать со свекольным соком и в одинаковых пропорциях с мёдом. Только пить не стаканами, а понемногу три раза в день.
Продукты повышающие гемоглобин в крови
Каждой клетке нашего тела чрезвычайно важно получать кислород. Диеты, сбои в питании, проблемы с пищеварением, стресс могут привести к снижению уровня гемоглобина и, как следствие, нарушению нормального доступа кислорода. Что скушать для стабилизации показателя, про какие витамины не стоит забывать и как проверить свой уровень белка в крови расскажем сегодня.
Разбор понятий.
Гемоглобин – это особый вид белка, который содержит в себе железо и, благодаря своей способности синтезироваться с кислородом, выполняет одну из важнейших функций в организме – перенос кислорода ко всем клеточкам и тканям вместе с кровообращением. Чем ниже в организме уровень гемоглобина, тем меньшее количество к клеткам поступает кислорода, что негативно сказывается на состоянии здоровья.
Чем ниже в организме уровень гемоглобина, тем меньшее количество к клеткам поступает кислорода, что негативно сказывается на состоянии здоровья.
Возможные симптомы низкого уровня гемоглобина.
- усталость, сильный упадок сил
- одышка
- синеватые губы и ногти
- похудение/тошнота/изжога
- бледность кожи
- тремор рук
- мушки в глазах и головокружения
- кисти рук и ступни постоянно мерзнут
- непонятная страсть к резким запахам
- желание погрызть мел, лед
Низкий гемоглобин (анемия) – довольно опасное состояние организма, это может привести к необратимым последствиям. Если вы начали отмечать за собой эти признаки, то советуем сходить и сдать анализ крови.
Если вам не хочется высчитывать суточную норму железа и, исходя их этого, формировать рацион, можно просто начать принимать комплекс витаминов В. В данном разделе вы сможете подобрать себе понравившиеся продукты и витамины, все они способствуют улучшению состояния крови.
Перейти в каталог
Правильное решение.
Гемоглобин, норма которого для мужчин, женщин и детей разнится, легко привести в порядок, если вовремя заметить проблему. Первое и самое действенное оружие – изменить свой рацион, привнести в него все нужные полезные витамины и микроэлементы, которые наполнят клетки железом в должной норме. Особенно внимательно за уровнем гемоглобина должны следить вегетарианцы и веганы, так как все остальные чаще всего повышают свою норму за счет употребления мясных продуктов и субпродуктов.
Читайте также: Дефицит витамина В12. Симптомы. Причины. Лечение.
Как повысить гемоглобин?
Если у вас диагностировали железодефицитную анемию, то придется употреблять продукты с высоким содержанием витамина B, а также витамины и препараты железа. Хорошо улучшают состояние:
- Халва, она состоит из переработанных зерен кунжута, либо подсолнечника, которые славятся содержанием в них железа.

- Также много железа в красной свекле – употребляйте ее в виде сока, добавляйте в салаты,
- Из рябины можно готовить настойки, яблоках – полезно ежедневное употребление вместе с косточками, отваре шиповника, гранате и натуральном гранатовом соке.
- В холодное время года смесь меда с грецкими орехами защитит не только от простуд, но и также поможет держать стабильный уровень гемоглобина.
Гемоглобин в крови. Советы врачей.
Будьте внимательны к себе!
Молекула месяца: гемоглобин
Красная кровь, голубая кровь
Вы когда-нибудь задумывались, почему кровеносные сосуды кажутся синими? Кислородная кровь ярко-красная: когда вы режетесь, кровь, которую вы видите, — это ярко-красная насыщенная кислородом кровь. Деоксигенированная кровь темно-фиолетового цвета: когда вы сдаете кровь или сдаете образец крови в кабинете врача, она втягивается в трубку для хранения вдали от кислорода, поэтому вы можете видеть этот темно-фиолетовый цвет. Тем не менее, темно-фиолетовая дезоксигенированная кровь кажется синей, поскольку течет по нашим венам, особенно у людей со светлой кожей.Это связано с тем, как свет разных цветов проходит через кожу: синий свет отражается в поверхностных слоях кожи, а красный свет проникает глубже. Темная кровь в вене поглощает большую часть этого красного света (а также любого синего света, который проникает так далеко), поэтому мы видим синий свет, который отражается от поверхности кожи. С другой стороны, некоторые организмы, такие как улитки и крабы, используют медь для переноса кислорода, поэтому у них действительно голубая кровь.
Тем не менее, темно-фиолетовая дезоксигенированная кровь кажется синей, поскольку течет по нашим венам, особенно у людей со светлой кожей.Это связано с тем, как свет разных цветов проходит через кожу: синий свет отражается в поверхностных слоях кожи, а красный свет проникает глубже. Темная кровь в вене поглощает большую часть этого красного света (а также любого синего света, который проникает так далеко), поэтому мы видим синий свет, который отражается от поверхности кожи. С другой стороны, некоторые организмы, такие как улитки и крабы, используют медь для переноса кислорода, поэтому у них действительно голубая кровь. Гемоглобин — это белок, который делает кровь красной.Он состоит из четырех белковых цепей, двух альфа-цепей и двух бета-цепей, каждая с кольцеобразной гемовой группой, содержащей атом железа. Кислород обратимо связывается с этими атомами железа и переносится через кровь. Каждая из белковых цепей похожа по структуре на миоглобин, белок, используемый для хранения кислорода в мышцах и других тканях. Однако четыре цепи гемоглобина дают ему некоторые дополнительные преимущества, как описано ниже.
Однако четыре цепи гемоглобина дают ему некоторые дополнительные преимущества, как описано ниже.
Использование и злоупотребление гемоглобином
Помимо транспорта кислорода, гемоглобин может связывать и переносить другие молекулы, такие как оксид азота и оксид углерода.Оксид азота влияет на стенки кровеносных сосудов, заставляя их расслабляться. Это, в свою очередь, снижает кровяное давление. Недавние исследования показали, что оксид азота может связываться со специфическими остатками цистеина в гемоглобине, а также с железами в гемовых группах, как показано в записи PDB 1buw . Таким образом, гемоглобин способствует регулированию артериального давления, распределяя оксид азота через кровь. С другой стороны, окись углерода — ядовитый газ. Он легко заменяет кислород в гемовых группах, как видно из записи PDB 2hco и многих других, образуя устойчивые комплексы, которые трудно удалить.Это злоупотребление гемовыми группами блокирует нормальное связывание и транспорт кислорода, удушая окружающие клетки.
Искусственная кровь
Переливания крови спасли бесчисленное количество жизней. Однако необходимость подбора группы крови, короткий срок хранения крови и возможность заражения по-прежнему вызывают серьезную озабоченность. Понимание того, как работает гемоглобин, основанное на десятилетиях биохимических исследований и многих кристаллографических структур, побудило к поиску кровезаменителей и искусственной крови.Самый очевидный подход — использовать раствор чистого гемоглобина для восполнения потерянной крови. Основная задача — сохранить вместе четыре белковые цепи гемоглобина. В отсутствие защитной оболочки эритроцита четыре цепи быстро распадаются. Чтобы избежать этой проблемы, были разработаны новые молекулы гемоглобина, в которых две из четырех цепей физически связаны вместе, как показано в записи PDB 1c7d . В этой структуре два дополнительных остатка глицина образуют связь между двумя цепями, предотвращая их разделение в растворе.Hemoglobin Cousins
Просматривая PDB, вы найдете много разных молекул гемоглобина. Вы можете найти новаторскую структуру гемоглобина лошади Макса Перуца в записи 2dhb , показанной на картинке здесь. Есть структуры гемоглобинов человека, как взрослого, так и эмбрионального. Вы также можете найти необычные гемоглобины, такие как леггемоглобин, который содержится в бобовых. Считается, что он защищает чувствительные к кислороду бактерии, которые фиксируют азот в корнях бобовых растений. В последние несколько лет были идентифицированы некоторые родственники гемоглобина, называемые «усеченными гемоглобинами», такие как гемоглобин в записи PDB 1idr , из которых несколько частей классической структуры были вырезаны.Единственная особенность, которая является абсолютно консервативной в этом подсемействе белков, — это аминокислота гистидин, которая связывается с гемовым железом.
Вы можете найти новаторскую структуру гемоглобина лошади Макса Перуца в записи 2dhb , показанной на картинке здесь. Есть структуры гемоглобинов человека, как взрослого, так и эмбрионального. Вы также можете найти необычные гемоглобины, такие как леггемоглобин, который содержится в бобовых. Считается, что он защищает чувствительные к кислороду бактерии, которые фиксируют азот в корнях бобовых растений. В последние несколько лет были идентифицированы некоторые родственники гемоглобина, называемые «усеченными гемоглобинами», такие как гемоглобин в записи PDB 1idr , из которых несколько частей классической структуры были вырезаны.Единственная особенность, которая является абсолютно консервативной в этом подсемействе белков, — это аминокислота гистидин, которая связывается с гемовым железом.Аллостерическое движение гемоглобина с молекулой кислорода бирюзового цвета.
Сотрудничество упрощает работу
Гемоглобин — замечательная молекулярная машина, которая использует движение и небольшие структурные изменения для регулирования своего действия. Связывание кислорода в четырех участках гема в гемоглобине не происходит одновременно. Как только первый гем связывает кислород, он вносит небольшие изменения в структуру соответствующей белковой цепи.Эти изменения подталкивают соседние цепи к другой форме, заставляя их легче связывать кислород. Таким образом, сложно добавить первую молекулу кислорода, но связывание второй, третьей и четвертой молекул кислорода становится все легче и легче. Это дает большое преимущество в функции гемоглобина. Когда кровь находится в легких, где много кислорода, кислород легко связывается с первой субъединицей, а затем быстро заполняет остальные. Затем, когда кровь циркулирует по телу, уровень кислорода падает, а уровень углекислого газа увеличивается.В этой среде гемоглобин выделяет связанный кислород. Как только первая молекула кислорода отпадает, белок начинает менять свою форму. Это побуждает к быстрому высвобождению оставшихся трех атомов кислорода. Таким образом, гемоглобин улавливает максимально возможную нагрузку кислорода в легких и доставляет его в нужное место и в нужное время.
Связывание кислорода в четырех участках гема в гемоглобине не происходит одновременно. Как только первый гем связывает кислород, он вносит небольшие изменения в структуру соответствующей белковой цепи.Эти изменения подталкивают соседние цепи к другой форме, заставляя их легче связывать кислород. Таким образом, сложно добавить первую молекулу кислорода, но связывание второй, третьей и четвертой молекул кислорода становится все легче и легче. Это дает большое преимущество в функции гемоглобина. Когда кровь находится в легких, где много кислорода, кислород легко связывается с первой субъединицей, а затем быстро заполняет остальные. Затем, когда кровь циркулирует по телу, уровень кислорода падает, а уровень углекислого газа увеличивается.В этой среде гемоглобин выделяет связанный кислород. Как только первая молекула кислорода отпадает, белок начинает менять свою форму. Это побуждает к быстрому высвобождению оставшихся трех атомов кислорода. Таким образом, гемоглобин улавливает максимально возможную нагрузку кислорода в легких и доставляет его в нужное место и в нужное время.
На этом анимированном рисунке гемовая группа одной субъединицы, показанная в маленьком круглом окошке, хранится в одном месте, так что вы можете видеть, как белок перемещается вокруг нее при связывании кислорода.Молекула кислорода показана сине-зеленым цветом. Когда он связывается с атомом железа в центре гема, он тянет аминокислоту гистидин вверх на нижней стороне гема. Это смещает положение всей альфа-спирали, показанной здесь оранжевым цветом под гемом. Это движение распространяется по всей белковой цепи и на другие цепи, в конечном итоге вызывая большое качательное движение двух субъединиц, показанных синим цветом. Показаны две структуры: записи PDB 2hhb и 1hho .
Проблемные гемоглобины
Гены белковых цепей гемоглобина имеют небольшие различия в разных человеческих популяциях, поэтому аминокислотная последовательность гемоглобина немного отличается от человека к человеку. В большинстве случаев изменения не влияют на функцию белков и часто даже не замечаются. Однако в некоторых случаях эти разные аминокислоты приводят к серьезным структурным изменениям. Одним из таких примеров является гемоглобин серповидных клеток, где глутамат 6 в бета-цепи мутирован в валин.Это изменение позволяет деоксигенированной форме гемоглобина прилипать друг к другу, как показано в записи PDB 2hbs , производя жесткие волокна гемоглобина внутри красных кровяных телец. Это, в свою очередь, деформирует эритроцит, который обычно представляет собой гладкий диск, в форму С или серпа. Деформированные клетки хрупкие и часто разрываются, что приводит к потере гемоглобина. Это может показаться ужасной вещью, но в одном случае это действительно преимущество. Паразиты, вызывающие тропическую болезнь малярию, которые проводят часть своего жизненного цикла в красных кровяных тельцах, не могут жить в серповидных клетках, заполненных клетчаткой.Таким образом, люди с серповидноклеточным гемоглобином в некоторой степени устойчивы к малярии. Другие обстоятельства, приводящие к проблемным гемоглобинам, возникают из-за несоответствия в производстве альфа- и бета-белков.
Однако в некоторых случаях эти разные аминокислоты приводят к серьезным структурным изменениям. Одним из таких примеров является гемоглобин серповидных клеток, где глутамат 6 в бета-цепи мутирован в валин.Это изменение позволяет деоксигенированной форме гемоглобина прилипать друг к другу, как показано в записи PDB 2hbs , производя жесткие волокна гемоглобина внутри красных кровяных телец. Это, в свою очередь, деформирует эритроцит, который обычно представляет собой гладкий диск, в форму С или серпа. Деформированные клетки хрупкие и часто разрываются, что приводит к потере гемоглобина. Это может показаться ужасной вещью, но в одном случае это действительно преимущество. Паразиты, вызывающие тропическую болезнь малярию, которые проводят часть своего жизненного цикла в красных кровяных тельцах, не могут жить в серповидных клетках, заполненных клетчаткой.Таким образом, люди с серповидноклеточным гемоглобином в некоторой степени устойчивы к малярии. Другие обстоятельства, приводящие к проблемным гемоглобинам, возникают из-за несоответствия в производстве альфа- и бета-белков. Структура требует равного производства обоих белков. Отсутствие одного из этих белков приводит к состоянию, называемому талассемией.
Структура требует равного производства обоих белков. Отсутствие одного из этих белков приводит к состоянию, называемому талассемией.Гемоглобин — обзор | Темы ScienceDirect
21.2 Реакции, запрещенные спином
Реакции, запрещенные спином, имеют реагенты и продукты разного спина, поэтому для них требуется запрещенное по симметрии пересечение от одной энергетической поверхности к другой.Для молекул, содержащих только легкие атомы, реакции пересечения спинов практически невозможны. Напротив, соединения переходных металлов часто имеют несколько низколежащих возбужденных состояний с различными конфигурациями неспаренных электронов. Многочисленные возбужденные состояния создают больше возможностей для спин-пересечений, а высокая спин-орбитальная связь для переходных металлов [10] делает пересечение более вероятным при каждой возможности.
Скорость реакции пересечения спинов зависит как от спин-орбитального взаимодействия, так и от вероятности того, что система посетит «шов» между состояниями спина. Шов — это пересечение диабатических спиновых состояний. Как показано на рисунке 21.2.1, шов имеет ту же размерность, что и разделяющая поверхность (3N-1, где N — количество атомов). Для теории (адиабатического) переходного состояния седловая точка была особенно важной точкой на разделяющей поверхности. Точно так же для неадиабатической теории пересечения спинов точка пересечения с минимальной энергией (MECP) является особенно важной точкой на стыке. Общая скорость реакции пересечения спинов также зависит от положения MECP относительно других характеристик энергетического ландшафта (ов).
Шов — это пересечение диабатических спиновых состояний. Как показано на рисунке 21.2.1, шов имеет ту же размерность, что и разделяющая поверхность (3N-1, где N — количество атомов). Для теории (адиабатического) переходного состояния седловая точка была особенно важной точкой на разделяющей поверхности. Точно так же для неадиабатической теории пересечения спинов точка пересечения с минимальной энергией (MECP) является особенно важной точкой на стыке. Общая скорость реакции пересечения спинов также зависит от положения MECP относительно других характеристик энергетического ландшафта (ов).
Рисунок 21.2.1. (Слева) Схематическое изображение диабатов, шва и MECP в системе с двумя степенями свободы. MECP слева отделяет реагенты на одной спиновой поверхности от продуктов на другой спиновой поверхности. (Справа) Одномерная схема спин-скрещивания на пути от триплетной версии вида A ( 3 A ) к пятимерной версии вида B ( 5 B ) . Поскольку MECP по существу является частью бассейнов ( 3 A ) и ( 5 A ), спин-кроссинг не сразу приводит к 5 B .Если переходное состояние на поверхности пятерки на несколько k B T выше MECP, ограничивающим шагом все же может быть обычная скорость пересечения 5 ‡.
Поскольку MECP по существу является частью бассейнов ( 3 A ) и ( 5 A ), спин-кроссинг не сразу приводит к 5 B .Если переходное состояние на поверхности пятерки на несколько k B T выше MECP, ограничивающим шагом все же может быть обычная скорость пересечения 5 ‡.
Швы часто изображаются как максимумы вдоль пути реакции, но они также могут располагаться рядом с геометрией реагента на двух поверхностях, рядом с геометрией продукта или даже за пределами области между реагентами и продуктами. Как показано на рис. 21.2.1, маршруты спуска от раннего (или позднего) MECP на двух спиновых поверхностях могут привести к схожим видам с разным вращением.В зависимости от места пересечения спинов преобразование реагента в продукт другого спина может потребовать как перекрестного спина, так и (адиабатического) прохождения через седло на одной из спиновых поверхностей.
Когда MECP является максимальным на пути от реагентов к намеченным продуктам, скорость пересечения шва определяет скорость для элементарного шага. На рисунке 21.2.2 показаны величины, которые будут важны при вычислении скорости пересечения спинов.
На рисунке 21.2.2 показаны величины, которые будут важны при вычислении скорости пересечения спинов.
Рисунок 21.2.2. Диабатические поверхности для запрещенной по спину реакции получаются из типичных расчетов электронной структуры без спин-орбитальной связи. V 12 — сила спин-орбитальной связи. Обратите внимание, что MECP находится чуть выше седловой точки, которая возникла бы на адиабатической поверхности основного состояния, если бы было включено спин-орбитальное взаимодействие. [По материалам Harvey Phys. Chem. Chem. Phys . 9, 331-43 (2007).]
Расчет неадиабатической скорости требует частоты достижения шва, а также вероятности перехода от одной поверхности к другой при прохождении траектории через шов. Ландау [11] и Зинер [12] вывели вероятность скачка с одной адиабатической поверхности на другую.Вероятность, которую мы хотим, состоит в том, что для прыжка с одной поверхности diabatic на другую, когда траектория пересекает шов. Таким образом, вероятность неадиабатического перехода равна PNA = 1 − PLZ, где PLZ — результат Ландау-Зинера. Ключевыми параметрами теории Ландау-Зинера являются абсолютная скорость | q˙ | перпендикулярно шву величина спин-орбитальной связи | V12 | на шве, и разница в градиентах на двух диабатических поверхностях в направлении, перпендикулярном шву, т.е.е. ∂E1 / ∂q − ∂E2 / ∂q. Вероятность неадиабатического перехода для одного пересечения шва составляет
Таким образом, вероятность неадиабатического перехода равна PNA = 1 − PLZ, где PLZ — результат Ландау-Зинера. Ключевыми параметрами теории Ландау-Зинера являются абсолютная скорость | q˙ | перпендикулярно шву величина спин-орбитальной связи | V12 | на шве, и разница в градиентах на двух диабатических поверхностях в направлении, перпендикулярном шву, т.е.е. ∂E1 / ∂q − ∂E2 / ∂q. Вероятность неадиабатического перехода для одного пересечения шва составляет
(21.2.1) PNA = 1 − exp [−θ (| q˙ |)]
, где параметр Месси θ (| q˙ |) равен
(21.2.2) θ = 2π | V12 | 2ħ | q˙∂ (E2 − E1) / ∂q |
Уравнение (21.2.1) основано на нескольких упрощающих предположениях: постоянная скорость на пересечении, постоянные уклоны двух поверхностей и постоянная связь. Тем не менее, он дает полуколичественную оценку вероятности неадиабатического перехода.Величины в параметре Месси показывают, что переход более вероятен для траекторий, которые проходят через шов медленно, для большой спин-орбитальной связи и для поверхностей, которые пересекаются с почти касательными наклонами. Медленная скорость пересечения и почти касательные поверхности сохраняют ситуацию, когда энергии двух спиновых состояний почти одинаковы в течение длительного интервала времени вдоль траектории пересечения шва. Длительное вырождение энергии создает большое окно возможностей для электронных степеней свободы, чтобы сделать переход с сохранением энергии.Обратите внимание, что небольшие изменения параметра Месси экспоненциально увеличиваются, что дает потенциально огромные изменения в вероятности неадиабатического пересечения. Вот почему могут происходить запрещенные по спину реакции при участии переходных металлов или почти параллельных пересечений [13].
Медленная скорость пересечения и почти касательные поверхности сохраняют ситуацию, когда энергии двух спиновых состояний почти одинаковы в течение длительного интервала времени вдоль траектории пересечения шва. Длительное вырождение энергии создает большое окно возможностей для электронных степеней свободы, чтобы сделать переход с сохранением энергии.Обратите внимание, что небольшие изменения параметра Месси экспоненциально увеличиваются, что дает потенциально огромные изменения в вероятности неадиабатического пересечения. Вот почему могут происходить запрещенные по спину реакции при участии переходных металлов или почти параллельных пересечений [13].
На этом этапе обычный вывод общей скорости пересечения пласта предполагает, что отклонение пересечения пласта от состояния реагента будет включать два коррелированных пересечения пласта. Вероятность перехода при первом проходе по шву — ПНА.Вероятность переключения на втором проходе равна (1-PNA) PNA, то есть вероятность отсутствия перехода на первом проходе, умноженная на вероятность последующего прохода на обратном пути к минимуму в состоянии 1 [8]. Тогда предполагается, что общая вероятность равна PNA + (1-PNA) PNA или, что эквивалентно, PNA (2-PNA). Ключевые предположения в этом расчете состоят в том, что два пересечения происходят в местах с одинаковыми | ∂E2 / ∂q − ∂E1 / ∂q | и с теми же абсолютными скоростями по q . Можно избежать этих предположений, как показано в выводе ниже.
Тогда предполагается, что общая вероятность равна PNA + (1-PNA) PNA или, что эквивалентно, PNA (2-PNA). Ключевые предположения в этом расчете состоят в том, что два пересечения происходят в местах с одинаковыми | ∂E2 / ∂q − ∂E1 / ∂q | и с теми же абсолютными скоростями по q . Можно избежать этих предположений, как показано в выводе ниже.
Частота перехода из состояния 1 в состояние 2 на пересечении составляет
(21.2.3) kNA = 〈δ [q − q ×] | q | ˙PNA (| q | ˙)〉 1 = ∫dq∫ dq˙e − β (F1 (q) + mq˙2 / 2) δ [q − q ×] | q˙ | PNA (| q˙ |) ∫dq∫dq˙e − β (F1 (q) + mq ˙2 / 2)
где × обозначает точку пересечения, а нижний индекс 1 указывает, что среднее значение превышает диабатическое состояние 1. Уравнение (21.2.3) точно количественно определяет вероятность достижения любой точки на шве при q (x) = q ×, но локальная разность сил | ∂E2 / ∂q − ∂E1 / ∂q | может отличаться от одной точки шва к другой.Неясно, насколько важны результирующие вариации параметра Месси, но они обычно игнорируются. Помимо этого приближения, уравнение (21.2.3) учитывает (1) вероятность выхода на шов, (2) абсолютную скорость траектории, проходящей через шов, и (3) вероятность перехода с одной поверхности на другой. В этой формуле переходы могут происходить при пересечении траекторий в любом направлении.
Помимо этого приближения, уравнение (21.2.3) учитывает (1) вероятность выхода на шов, (2) абсолютную скорость траектории, проходящей через шов, и (3) вероятность перехода с одной поверхности на другой. В этой формуле переходы могут происходить при пересечении траекторий в любом направлении.
При достаточно слабой связи | V12 | параметр Месси будет мал для всех типичных скоростей в пласте.Для первого порядка по θ вероятность пересечения кривой для одного прохода через шов составляет
(21.2.4) PNA (| q | ˙) ≈θ (| q˙ |)
Также предположим, что свободная энергия профиль локально параболический около состояния реагента, т.е. около минимума в диабате 1:
(21.2.5) F1 (q) ≈m1ω12 (q − q10) 2/2
Подставляя приближения (21.2.4) и (21.2 .5) в уравнение (21.2.3), а затем завершение интегралов дает
(21.2.6) kNA = | V12 | 22πmω12 / kBTħ | ∂E2 / ∂q − ∂E1 / ∂q | exp [−F1 (q ×) kBT]
Скорость теперь экспоненциально зависит от F1 (q ×), свободной энергии на пересечении q × относительно минимума свободной энергии в состоянии реагента. Обратите внимание, что гармоническое приближение использовалось только в минимуме реагента. Свободную энергию в шве можно вычислить отдельно, например со стандартными статистическими суммами, в которых направление взаимного градиента было удалено из анализа колебаний в MECP.
Обратите внимание, что гармоническое приближение использовалось только в минимуме реагента. Свободную энергию в шве можно вычислить отдельно, например со стандартными статистическими суммами, в которых направление взаимного градиента было удалено из анализа колебаний в MECP.
Формально для вычисления F1 (q ×) требуется координата реакции q , для которой q = q × совпадает со швом. Для пересекающихся поверхностей больших размеров сразу видно, что q должно быть энергетической щелью и что q × = 0.Шов представляет собой набор всех конфигураций, для которых q = E2 (x) −E1 (x) = 0. Энергетическая щель широко использовалась в теоретической работе Маркуса, а также в вычислительной работе Варшела — таким образом, координата энергетической щели равна частично ответственны за две Нобелевские премии !
Пример: гемоглобин и триплет O
2 Связывание кислорода с гемоглобином включает переход триплета в синглет. Свободный кислород — это триплет, поэтому он должен быть химически инертным и недоступным для метаболизма. Чтобы хемосорбировать кислород в синглетном состоянии, должен произойти переход спин-состояние. Дженсен и Райд [14] показали, что гемоглобин имеет триплетные и синглетные поверхности с почти равной энергией в широкой пространственной области входного канала. По их оценкам, эта особенность диабатических энергетических ландшафтов увеличивает скорость связывания триплетного кислорода с гемом в 10 11 раз по сравнению с аналогичными неферментативными комплексами FeO [14]. Таким образом, наш метаболизм представляет собой своего рода контролируемый огонь — мы производим ровно столько гемоглобина, чтобы поддерживать его горение с оптимальной скоростью.
Чтобы хемосорбировать кислород в синглетном состоянии, должен произойти переход спин-состояние. Дженсен и Райд [14] показали, что гемоглобин имеет триплетные и синглетные поверхности с почти равной энергией в широкой пространственной области входного канала. По их оценкам, эта особенность диабатических энергетических ландшафтов увеличивает скорость связывания триплетного кислорода с гемом в 10 11 раз по сравнению с аналогичными неферментативными комплексами FeO [14]. Таким образом, наш метаболизм представляет собой своего рода контролируемый огонь — мы производим ровно столько гемоглобина, чтобы поддерживать его горение с оптимальной скоростью.
Спин-орбитальное взаимодействие в комплексах переходных металлов часто составляет от 10 до 100 см – 1 [10]. Неадиабатические спин-запрещенные реакции наиболее важны для переходных металлов 3d и 4d [13]. Для металлов 4f, 5d и 5f спин-орбитальное взаимодействие настолько велико, что реакции, включающие изменение спина, могут по существу протекать адиабатически [13].
Было разработано несколько алгоритмов для поиска MECP [15–17]. Самый простой — минимизировать L = E1 − λ (E2 − E1) относительно положений атомов и множителя Лагранжа λ [15].Вычислительные исследования запрещенных по спину реакций в основном сосредоточены на газофазных реакциях, но также проводился анализ реакций с запрещенными по спину реакций в ферментах, гомогенном и гетерогенном катализе. См. Прекрасные обзоры теории, вычислительных методов и приложений вычислений пересечения спинов у Харви и его сотрудников [8,18].
Гемоглобин и функции железа | Обучение пациентов
Железо — важный элемент для производства крови. Около 70 процентов железа в вашем организме содержится в красных кровяных тельцах, называемых гемоглобином, и в мышечных клетках, называемых миоглобином.Гемоглобин необходим для переноса кислорода в крови от легких к тканям. Миоглобин в мышечных клетках принимает, хранит, транспортирует и выделяет кислород.
Около 6 процентов железа в организме является компонентом определенных белков, необходимых для дыхания и энергетического обмена, а также как компонент ферментов, участвующих в синтезе коллагена и некоторых нейротрансмиттеров. Железо также необходимо для правильной работы иммунной системы.
Железо также необходимо для правильной работы иммунной системы.
Около 25 процентов железа в организме хранится в виде ферритина, содержится в клетках и циркулирует в крови.Средний взрослый мужчина имеет около 1000 мг запасенного железа (достаточно примерно на три года), тогда как женщины в среднем имеют только около 300 мг (достаточно примерно на шесть месяцев). Когда потребление железа хронически низкое, запасы железа могут истощаться, что снижает уровень гемоглобина.
Когда запасы железа истощены, это состояние называется истощением запасов железа. Дальнейшее снижение может быть названо железодефицитным эритропоэзом, и дальнейшее снижение вызывает железодефицитную анемию.
Кровопотеря — наиболее частая причина дефицита железа.У мужчин и женщин в постменопаузе дефицит железа почти всегда является результатом желудочно-кишечной кровопотери. У менструирующих женщин потеря крови из мочеполовой системы часто является причиной повышенной потребности в железе. Оральные контрацептивы, как правило, уменьшают менструальную кровопотерю, в то время как внутриматочные контрацептивы имеют тенденцию увеличивать менструальное кровотечение. Другие причины мочеполовых кровотечений и кровотечений из дыхательных путей также увеличивают потребность в железе.
Другие причины мочеполовых кровотечений и кровотечений из дыхательных путей также увеличивают потребность в железе.
Для доноров крови каждая сдача крови приводит к потере от 200 до 250 мг железа.В периоды роста в младенчестве, детстве и подростковом возрасте потребности в железе могут превышать поступление железа из рациона и запасов. Потеря железа из-за роста тканей во время беременности и из-за кровотечений во время родов и в послеродовом периоде составляет в среднем 740 мг. Грудное вскармливание увеличивает потребность в железе примерно на 0,5–1 мг в день.
Требования к железу
Ваш «уровень железа» проверяется перед каждой сдачей крови, чтобы определить, безопасно ли для вас сдавать кровь. Железо не вырабатывается в организме и должно усваиваться из того, что вы едите.Минимальная суточная потребность взрослого человека в железе составляет 1,8 мг. Только от 10 до 30 процентов потребляемого вами железа усваивается и используется организмом.
Суточная потребность в железе может быть достигнута за счет приема добавок железа. Сульфат железа 325 мг перорально один раз в день и с пищей с высоким содержанием железа. Также рекомендуются продукты с высоким содержанием витамина С, потому что витамин С помогает организму усваивать железо. Приготовление пищи в чугунных кастрюлях может добавить к пище до 80 процентов больше железа. Перед приемом добавок железа проконсультируйтесь с вашим лечащим врачом.
Сульфат железа 325 мг перорально один раз в день и с пищей с высоким содержанием железа. Также рекомендуются продукты с высоким содержанием витамина С, потому что витамин С помогает организму усваивать железо. Приготовление пищи в чугунных кастрюлях может добавить к пище до 80 процентов больше железа. Перед приемом добавок железа проконсультируйтесь с вашим лечащим врачом.
Некоторые продукты, богатые железом, включают:
Мясо и птица
- Постная говядина
- Телятина
- Свинина
- Баранина
- Цыпленок
- Турция
- Печень (кроме печени рыбы)
Морепродукты
Овощи
- Зелень всякая
- Тофу
- Брокколи
- Душистый горошек
- Брюссельская капуста
- Кале
- Ростки фасоли
- Помидоры
- Лимская фасоль
- Картофель
- Зеленая фасоль
- Кукуруза
- Свекла
- Капуста
Высокое содержание гемоглобина: причины, лечение
Обзор
Почему важен гемоглобин A1c.
Что такое высокий уровень гемоглобина?
Гемоглобин — это белок красных кровяных телец, который помогает крови переносить кислород по всему телу. (Гемоглобин содержит железо, которое придает крови красный цвет.) Подсчет гемоглобина — это косвенное измерение количества красных кровяных телец в вашем теле. Когда уровень гемоглобина выше нормы, это может быть признаком проблемы со здоровьем.
Нормальный уровень гемоглобина составляет от 14 до 17 г / дл (граммов на децилитр) для мужчин и от 12 до 15 г / дл для женщин.Уровни гемоглобина зависят от многих факторов, включая возраст, расу, пол и общее состояние здоровья человека.
Гемоглобин обычно измеряется как часть общего анализа крови (стандартный анализ крови) вместе с гематокритом (процентное содержание эритроцитов в крови), чтобы помочь диагностировать заболевания и узнать больше о здоровье человека. .
Симптомы и причины
Что может вызвать повышенный уровень гемоглобина?
Многие факторы могут влиять на уровень гемоглобина. Иногда высокий уровень гемоглобина является результатом образа жизни или побочным эффектом приема лекарств.
Иногда высокий уровень гемоглобина является результатом образа жизни или побочным эффектом приема лекарств.
Заболевания, которые могут вызвать высокий уровень гемоглобина, включают:
- Истинная полицитемия (костный мозг производит слишком много красных кровяных телец)
- Заболевания легких, такие как ХОБЛ, эмфизема или фиброз легких (на легочной ткани появляются рубцы)
- Порок сердца, особенно врожденный порок сердца (с ним рождается ребенок)
- Опухоли почек
- Обезвоживание (от диареи или недостатка жидкости)
- Гипоксия (низкий уровень кислорода в крови)
- Воздействие окиси углерода (обычно связанное с курением)
Факторы образа жизни, которые могут вызвать высокий уровень гемоглобина, включают:
- Курение сигарет
- Жизнь на большой высоте
- Прием препаратов, улучшающих работоспособность, таких как анаболические стероиды (например, синтетический тестостерон) или эритропоэтин
Диагностика и тесты
Чего мне ожидать, если мой врач обнаружит высокий уровень гемоглобина?
Врачи обычно обнаруживают высокий уровень гемоглобина при проведении тестов на другое заболевание. Ваш врач может провести дополнительные тесты, чтобы определить причину повышенного уровня гемоглобина. Эти тесты могут искать условия, при которых ваше тело вырабатывает слишком много красных кровяных телец, или нарушения, ограничивающие поступление кислорода.
Ваш врач может провести дополнительные тесты, чтобы определить причину повышенного уровня гемоглобина. Эти тесты могут искать условия, при которых ваше тело вырабатывает слишком много красных кровяных телец, или нарушения, ограничивающие поступление кислорода.
Ведение и лечение
Как лечить высокий уровень гемоглобина?
Если заболевание вызывает высокий уровень гемоглобина, ваш врач может порекомендовать процедуру или лекарства для его снижения.
Во время процедуры, называемой флеботомией, медицинский работник вводит иглу в вашу вену и сливает кровь через трубку в мешок или контейнер.Возможно, вам придется повторять эту процедуру до тех пор, пока уровень гемоглобина не станет близким к норме.
Тест на гемоглобин
Обзор
Почему важен гемоглобин A1c.Что такое анализ гемоглобина?
Тест на гемоглобин измеряет количество гемоглобина в крови. Гемоглобин — это белок, который является основным компонентом красных кровяных телец (эритроцитов). Эритроциты производятся в костном мозге. Гемоглобин содержит железо, которое позволяет ему связываться с кислородом.Красные кровяные тельца переносят кислород из легких в другие ткани и органы. Они также переносят углекислый газ в легкие, чтобы его можно было удалить из организма.
Эритроциты производятся в костном мозге. Гемоглобин содержит железо, которое позволяет ему связываться с кислородом.Красные кровяные тельца переносят кислород из легких в другие ткани и органы. Они также переносят углекислый газ в легкие, чтобы его можно было удалить из организма.
Уровень гемоглобина ниже нормы, также известный как анемия, может указывать на то, что органы вашего тела не получают достаточного количества кислорода. Это может привести к нехватке энергии, усталости или другим проблемам.
Низкий уровень гемоглобина может быть признаком того, что костный мозг не производит достаточного количества эритроцитов или что клетки разрушаются быстрее, чем производятся.Хроническая кровопотеря также приводит к падению уровня гемоглобина и является одной из наиболее частых причин анемии.
Зачем делают анализ на гемоглобин?
Тест на гемоглобин может проводиться вместе с обычным физическим обследованием для оценки количества гемоглобина в крови. Это делается как часть общего анализа крови (CBC), который определяет количество эритроцитов, лейкоцитов и тромбоцитов в образце крови. Общий анализ крови также проводится при появлении симптомов низкого уровня гемоглобина, таких как усталость, слабость или головокружение.
Общий анализ крови также проводится при появлении симптомов низкого уровня гемоглобина, таких как усталость, слабость или головокружение.
Существует множество заболеваний, которые приводят к низкому уровню гемоглобина или анемии, в том числе:
- Недостаток железа, который почти всегда вызван кровопотерей
- Дефицит других питательных веществ, таких как витамин B12 или фолиевая кислота
- Внутренняя или внешняя кровопотеря в результате хирургического вмешательства, травмы, менструального кровотечения или кровотечения из желудочно-кишечного тракта
- Рак
- Талассемия, распространенное наследственное заболевание крови, вызванное генетическими мутациями в генах гемоглобина.Обычно это легкая форма, но тяжелые формы могут вызывать симптомы в детстве.
- Болезнь почек
- Аутоиммунные болезни
Симптомы, указывающие на низкий уровень эритроцитов, могут включать:
- Усталость
- Кожа бледная (бледность)
- Слабость
- Головокружение
- Одышка
- Холодные руки и ноги
Тест на гемоглобин может использоваться для скрининга анемии и других заболеваний крови, а также для отслеживания прогресса во время лечения. Можно только установить наличие анемии и степень ее тяжести. Тест не может определить причину аномального уровня гемоглобина. Требуются дополнительные тесты.
Можно только установить наличие анемии и степень ее тяжести. Тест не может определить причину аномального уровня гемоглобина. Требуются дополнительные тесты.
Некоторые состояния приводят к увеличению количества красных кровяных телец в организме, вызывая избыток гемоглобина в крови. Эти расстройства включают:
Слишком много красных кровяных телец может привести к сгущению крови и ее вялости. Густая кровь течет не так быстро, что может лишить органы кислорода.
Симптомы повышенного уровня эритроцитов могут включать
- Головные боли
- Затуманенное зрение или двоение в глазах
- Головокружение
- Зуд
- Сгустки крови
Детали теста
Какая подготовка необходима перед исследованием гемоглобина?
Анализ гемоглобина не требует специальной подготовки. Обычно это занимает всего несколько минут. Тест можно сделать в кабинете врача, медицинской лаборатории или других амбулаторных условиях.
Как проводится анализ гемоглобина?
Потребуется образец крови. Небольшая игла вводится в вену, обычно в руку или руку. При необходимости кровь может быть взята из другой части тела. У детей для взятия крови можно использовать палочку из пальца. Новорожденным можно делать пяточную палку.
Перед забором крови медицинский работник промоет кожу около пораженного участка спиртом. Он или она обернет эластичную ленту вокруг вашего плеча и попросит вас сжать кулак, чтобы облегчить кровоток.Вы можете испытывать легкую боль или дискомфорт при введении иглы. Ваша кровь будет собрана в небольшой флакон или флаконы и отправлена в лабораторию для анализа.
Область вокруг прокола может казаться синяком или опухшей в течение нескольких дней.
Риски, связанные с тестом на гемоглобин, очень малы. В большинстве случаев значительных последствий не наблюдается.
Результаты и дальнейшие действия
На что указывают результаты теста?
Нормальный диапазон уровней гемоглобина — от 12 до 17. 4 грамма на децилитр крови для взрослых. Однако уровни могут варьироваться в зависимости от возраста и расы человека. Высота также может повлиять на результаты.
4 грамма на децилитр крови для взрослых. Однако уровни могут варьироваться в зависимости от возраста и расы человека. Высота также может повлиять на результаты.
Какое наблюдение требуется?
Ваш врач обсудит с вами результаты теста на гемоглобин. Врач может назначить дополнительные анализы, в зависимости от их результата. Лечение будет зависеть от основного состояния. Вам следует обсудить варианты лечения со своим врачом. Возможно, вам придется регулярно сдавать анализы на гемоглобин, если вы проходите курс лечения заболевания крови.
Гемоглобин— Общий анализ крови
Гемоглобин — Общий анализ кровиГемоглобин
гемоглобин
представляет собой молекулу, состоящую из четырех субъединиц. Каждая субъединица содержит железо, содержащее
пигмент (гем) и белок (глобулин). Есть два типа субъединиц: альфа
и бета. Каждый грамм гемоглобина может нести 1,34 мл кислорода. Кислород, несущий
способность крови прямо пропорциональна концентрации в ней гемоглобина. В
количество эритроцитов не указывает на содержание кислорода в крови, потому что
некоторые клетки могут содержать больше гемоглобина, чем другие. Определение гемоглобина
используется для скрининга на анемию, для определения степени анемии и для помощи
при оценке реакции пациента на терапию анемии. Гемоглобин также служит
как важный буфер pH во внеклеточной жидкости.
В
количество эритроцитов не указывает на содержание кислорода в крови, потому что
некоторые клетки могут содержать больше гемоглобина, чем другие. Определение гемоглобина
используется для скрининга на анемию, для определения степени анемии и для помощи
при оценке реакции пациента на терапию анемии. Гемоглобин также служит
как важный буфер pH во внеклеточной жидкости.
| Глюкоза
необратимо присоединяется к гемоблобину и другим контактам с белками. |
Снижение гемоглобина:
Кровопотеря и костный мозг
подавление снижает общее количество эритроцитов и, следовательно, снижает общее содержание гемоглобина.
Уровни гемоглобина также снижаются у пациентов с аномальными
типы гемоглобина или гемоглобинопатии. Красные кровяные тельца с аномальными типами
гемоглобина часто хрупкие и легко повреждаются или разрушаются в сосудах.
система. Электрофорез гемоглобина позволяет различать определенные типы аномальных
гемоглобин.
Красные кровяные тельца с аномальными типами
гемоглобина часто хрупкие и легко повреждаются или разрушаются в сосудах.
система. Электрофорез гемоглобина позволяет различать определенные типы аномальных
гемоглобин.
Талассемия передается по наследству рецессивная гемоглобинопатия. Это происходит из-за неспособности произвести достаточное количество молекулы глобина. Сбой может быть либо в альфа-, либо в бета-части. В серповидноклеточная анемия, у пациента гемоглобин неправильной формы, известный как серповидный гемоглобин (hgbS).Гемоглобин серпа создает деформированные эритроциты, которые образуют засоры в сосудах.
Остальные пациенты в норме Количество эритроцитов , но низкий уровень гемоглобина. Такая ситуация возникает при дефиците железа.
анемия, при которой в эритроцитах содержится меньше гемоглобина, чем обычно. Дефицит железа
анемию также называют гипохромной анемией. Гипохромный — это термин, который
означает «цвет меньше обычного». В целом женщинам нужно больше железа в
их диеты, чем у мужчин, из-за регулярной потери железа с менструальными выделениями.Во время беременности потребность женщины в железе для увеличения гемоглобина увеличивается.
Если женщина забеременеет при низких запасах железа, она подвергается риску
становится тяжелой анемией. Регулярный анализ гемоглобина — важная часть
наблюдение за беременной женщиной. Во время последнего триместра беременности состояние, известное как
возникает «физиологическая анемия беременности». Это нормальное падение гемоглобина
значения являются результатом увеличения объема плазмы. Множественные заборы крови
Недоношенные дети — частая причина анемии.
В целом женщинам нужно больше железа в
их диеты, чем у мужчин, из-за регулярной потери железа с менструальными выделениями.Во время беременности потребность женщины в железе для увеличения гемоглобина увеличивается.
Если женщина забеременеет при низких запасах железа, она подвергается риску
становится тяжелой анемией. Регулярный анализ гемоглобина — важная часть
наблюдение за беременной женщиной. Во время последнего триместра беременности состояние, известное как
возникает «физиологическая анемия беременности». Это нормальное падение гемоглобина
значения являются результатом увеличения объема плазмы. Множественные заборы крови
Недоношенные дети — частая причина анемии.
Мгновенно Обратная связь:
Красный
клетки крови с аномальным гемоглобином легче повреждаются или разрушаются
чем клетки с нормальным гемоглобином.
Гемоглобин: критически низкий и высокие значения
- Значение гемоглобина ниже 5 г / дл может вызвать сердечная недостаточность
- Значение гемоглобина выше
20 г / дл может вызвать закупорку капилляров.
 за счет гемоконцентрации
за счет гемоконцентрации
Повышенный уровень гемоглобина находятся в любом состоянии, при котором количество циркулирующих эритроцитов поднимается выше нормы.Примеры состояний, связанных с повышением гемоглобина истинная полицитемия, тяжелые ожоги, хроническая обструктивная болезнь легких, и застойная сердечная недостаточность.
Подробнее информацию о анемии, рассмотрите возможность посещения АМЕРИКАНСКОГО ОБЩЕСТВА ГЕМАТОЛОГИИ
http://www.hemology.org/Patients/Other-Resources/Education-Book/5302.aspx
© RnCeus.com
Гемоглобин
Гемоглобин Пол Мэй
Бристольский университет, Великобритания
Также доступны: только HTML, Chime-Enhanced, JMol и версии.
Миоглобин и гемоглобин — переносчики кислорода
Большинство живых организмов выполняет дыхание, расщепление пищевых продуктов с выделением энергии в присутствии кислорода. Однако кислород не очень хорошо растворяется в воде, и поэтому для того, чтобы животные доставляли кислород от легких (или жабр) к мышцам, им требовалось развить эффективную молекулу, переносящую кислород. У позвоночных этими молекулами являются белки миоглобин и гемоглобин.
Однако кислород не очень хорошо растворяется в воде, и поэтому для того, чтобы животные доставляли кислород от легких (или жабр) к мышцам, им требовалось развить эффективную молекулу, переносящую кислород. У позвоночных этими молекулами являются белки миоглобин и гемоглобин.
Красные кровяные тельца (вверху) содержат гемоглобин. Кровь ярко-красного цвета (слева) из-за наличия оксигемоглобина. |
Гемоглобин (или гемоглобин, часто сокращенно Hb), содержащийся в красных кровяных тельцах, служит переносчиком кислорода в крови. Название гемоглобин происходит от гема и глобина , поскольку каждая субъединица гемоглобина представляет собой глобулярный белок со встроенной гемовой (или гемовой) группой.Каждая группа гема содержит атом железа, который отвечает за связывание кислорода. Наличие гемоглобина в крови увеличивает кислородную способность литра крови с 5 до 250 мл. Гемоглобин также играет важную роль в транспортировке углекислого газа из тканей обратно в легкие. Миоглобин, с другой стороны, расположен в мышце и служит резервным источником кислорода, а также способствует перемещению O 2 внутри мышцы.
Гемоглобин также играет важную роль в транспортировке углекислого газа из тканей обратно в легкие. Миоглобин, с другой стороны, расположен в мышце и служит резервным источником кислорода, а также способствует перемещению O 2 внутри мышцы.
Ленточная структура и заполнение пространства белка гемоглобина | Структура палочки и заполнение пространства белка миоглобина |
Гем-порфирин
Хотя молекулы гемоглобина и миоглобина представляют собой очень большие сложные белки, активный центр на самом деле представляет собой небелковую группу, называемую гемом.Гем состоит из плоского органического кольца, окружающего атом железа. Органическая часть представляет собой порфириновое кольцо на основе порфина (тетрапиррольное кольцо) и является основой ряда других важных биологических молекул, таких как хлорофилл и цитохром. Кольцо содержит большое количество сопряженных двойных связей, что позволяет молекуле поглощать свет в видимой части спектра. Атом железа и присоединенная к нему белковая цепь изменяют длину волны поглощения и придают гемоглобину характерный цвет.Оксигенированный гемоглобин (обнаруженный в крови из артерий) ярко-красный, но без кислорода (как в крови из вен) гемоглобин становится более темно-красным. Венозная кровь часто изображается синим цветом на медицинских диаграммах, а вены иногда выглядят синими, если смотреть сквозь кожу. Появление крови как темно-синего цвета — это явление длины волны света, связанное с отражением синего света от внешней части венозной ткани, если вена имеет глубину ~ 0,02 дюйма или более.
Кольцо содержит большое количество сопряженных двойных связей, что позволяет молекуле поглощать свет в видимой части спектра. Атом железа и присоединенная к нему белковая цепь изменяют длину волны поглощения и придают гемоглобину характерный цвет.Оксигенированный гемоглобин (обнаруженный в крови из артерий) ярко-красный, но без кислорода (как в крови из вен) гемоглобин становится более темно-красным. Венозная кровь часто изображается синим цветом на медицинских диаграммах, а вены иногда выглядят синими, если смотреть сквозь кожу. Появление крови как темно-синего цвета — это явление длины волны света, связанное с отражением синего света от внешней части венозной ткани, если вена имеет глубину ~ 0,02 дюйма или более.
Порфин — строительный блок гема | |
Гем , небелковый активный сайт в миоглобине и гемоглобине.Боковые группы, которые были добавлены к порфину, выделены пурпурным цветом, а центральный атом железа показан красным. |
Обратимое связывание кислорода
Атом железа в геме связывается с 4 атомами азота в центре порфиринового кольца, но при этом остается два свободных места связывания для железа, по одному по обе стороны от плоскости гема. Гемовая группа расположена в щели в молекуле миоглобина и окружена неполярными остатками, за исключением двух полярных гистидинов.
Структура белка миоглобина |
Один из свободных участков связывания железа присоединяется к одному из этих гистидинов, оставляя последний участок связывания на другой стороне кольца доступным для связывания с кислородом. Вторая группа гистидина находится поблизости и служит нескольким целям. Он изменяет форму щели, так что только небольшие молекулы могут вступать в реакцию с атомом железа, а также помогает сделать реакцию обратимой, , так что кислород может высвобождаться, когда это необходимо соседним тканям. Удивительно осознавать, что вся сложная трехмерная структура большого белка миоглобина предназначена исключительно для создания щели точно правильной формы с правильными двумя группами гистидина в правильных положениях, чтобы облегчить обратимое поглощение кислорода.
Удивительно осознавать, что вся сложная трехмерная структура большого белка миоглобина предназначена исключительно для создания щели точно правильной формы с правильными двумя группами гистидина в правильных положениях, чтобы облегчить обратимое поглощение кислорода.
Схематическая диаграмма сайта связывания кислорода в миоглобине. |
Гемоглобин
Гемоглобин состоит из 4 единиц миоглобина, соединенных вместе, и его действие в отношении поглощения кислорода аналогичное, но более сложное.Когда мы дышим, кислород в легких проходит через тонкостенные кровеносные сосуды в красные кровяные тельца, где он связывается с гемоглобином, превращая его в ярко-красный оксигемоглобин. Затем кровь проходит по телу, пока не достигает клеток и тканей, которым необходим кислород для поддержания своих процессов. Эти клетки богаты CO 2 , который является побочным продуктом этих процессов. CO 2 вытесняет слабосвязанный O 2 и образует карбаминогемоглобин, который затем перемещается с кровотоком обратно в легкие, где снова замещается кислородом.
Ленточная диаграмма структуры гемоглобина . |
И O 2 , и CO 2 обратимо связывают с гемоглобином, но некоторые другие молекулы, такие как окись углерода, достаточно малы, чтобы поместиться в белковой щели, но образуют такие прочные связи с железом, что процесс составляет необратимый .Таким образом, высокие концентрации CO быстро расходуют ограниченные запасы молекул гемоглобина в организме и препятствуют их связыванию с кислородом. Вот почему CO ядовит — пострадавший быстро умирает от удушья, потому что его кровь больше не может переносить достаточно кислорода для снабжения тканей и мозга. Сродство связывания гемоглобина с CO в 200 раз больше, чем сродство к кислороду, а это означает, что небольшие количества CO резко снижают способность гемоглобинов переносить кислород. Когда гемоглобин соединяется с CO, он образует очень ярко-красное соединение, называемое карбоксигемоглобином.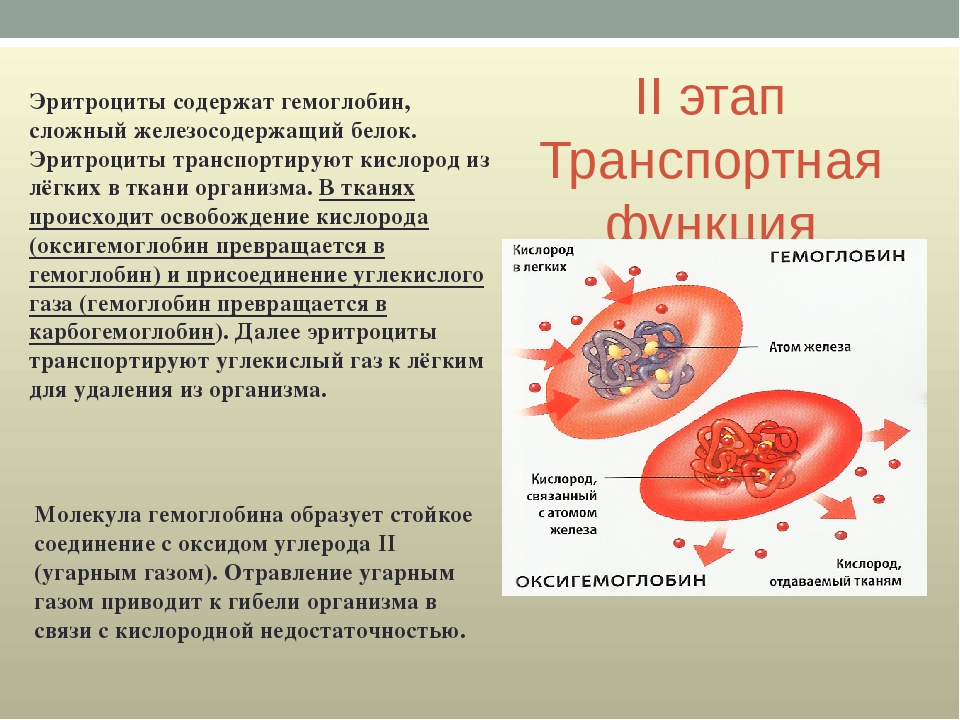 Когда вдыхаемый воздух содержит уровень CO всего 0,02%, возникают головная боль и тошнота. Если концентрация CO увеличится до 0,1%, наступит бессознательное состояние. У заядлых курильщиков до 20% активных центров кислорода может быть заблокировано CO. Другой ядовитой молекулой, которая связывается с гемоглобином, является цианистый водород (HCN). Как только цианид попадает в кровоток, большая часть (92-99%) связывается с гемоглобином в красных кровяных тельцах. Оттуда он попадает в ткани организма, где связывается с ферментом цитохромоксидазой и не дает клеткам использовать кислород.
Когда вдыхаемый воздух содержит уровень CO всего 0,02%, возникают головная боль и тошнота. Если концентрация CO увеличится до 0,1%, наступит бессознательное состояние. У заядлых курильщиков до 20% активных центров кислорода может быть заблокировано CO. Другой ядовитой молекулой, которая связывается с гемоглобином, является цианистый водород (HCN). Как только цианид попадает в кровоток, большая часть (92-99%) связывается с гемоглобином в красных кровяных тельцах. Оттуда он попадает в ткани организма, где связывается с ферментом цитохромоксидазой и не дает клеткам использовать кислород.
Артикул:
- Органическая химия , Моррисон и Бойд (Аллин и Бэкон, 1983).
- Биохимия , Л. Страйер (W.H. Freeman and Co, Сан-Франциско, 1975).
- Введение в органическую химию , Streitweiser and Heathcock (MacMillan, New York, 1981).
- Интерактивные трехмерные структуры гемоглобина — требуется Chime
- Википедия
Вернуться на страницу «Молекула месяца».

 ), Addison Wesley Longman, ISBN 0-8053-3066-6.
), Addison Wesley Longman, ISBN 0-8053-3066-6.
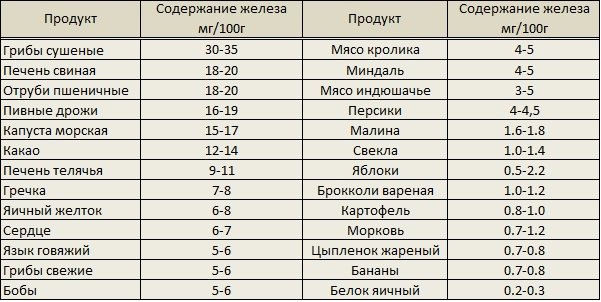
 за счет гемоконцентрации
за счет гемоконцентрации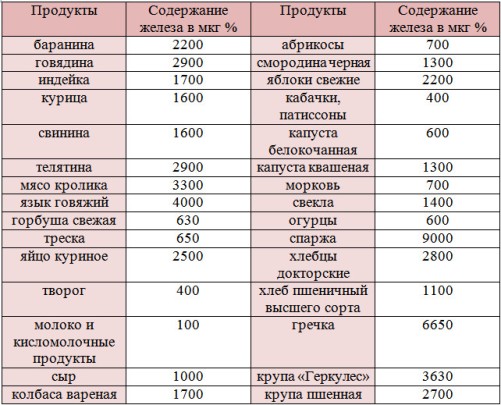
Добавить комментарий